研究内容【食品微生物学研究室】
全ての生物は細胞単位で生命活動を行い、基本的には共通の細胞機能により生命を維持している。
一方、微生物は地球上のあらゆる生物圏に生息し、それぞれの生息環境に適応することで独自の進化を遂げてきた。つまり、地球上には私たちの想像を遙かに超えた能力を持つ多種多様な微生物が生息している。
私たちのグループは、微生物を私たちの細胞機能解明のツールとして利用し、タンパク質および遺伝子など分子レベルで生命の神秘を解き明かす一方、未知の能力を持った微生物を自然界に広く求め、私たちの生活に応用することをめざしている。
酵母の細胞機能に関する研究
酵母は真核細胞であり、私達ヒトや植物などと同じ細胞構造・機能を保持している。
つまり、酵母をモデル生物として用いることでヒトや植物などの細胞機能を明らかにしていくことができる。また、出芽酵母をはじめ様々な酵母のゲノム配列が解明され、それに基づいた細胞機能解析が可能である。
私たちは様々な酵母を用いて、細胞のストレス応答、細胞内オルガネラの制御機構など、遺伝子・分子細胞学レベルでの様々な細胞機能を明らかにすることを目的にしている。特に、生物のアルデヒド・カルボニル化合物に対するストレス耐性機構の解明を目指している。
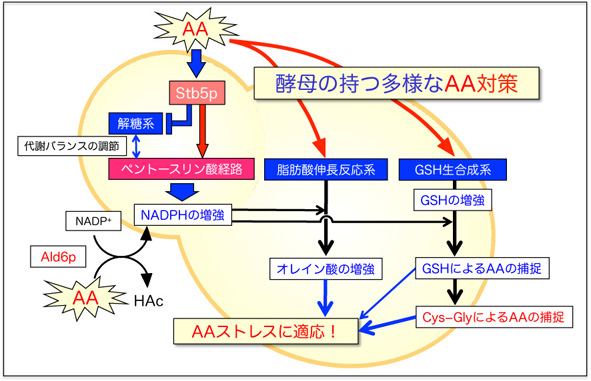
図. 出芽酵母のアセトアルデヒド耐性のメカニズム.
参考文献
中川智行. 2012. 出芽酵母のアセトアルデヒドに対する細胞応答と耐性機構. 日本醸造協会誌.107: 632-637.(総説)
Matsufuji Y, Yamamoto K, Yamauchi K, Mitsunaga T, Hayakawa T and Nakagawa T. 2013. The novel physiological roles for glutathione in sequestering acetaldehyde to confer acetaldehyde tolerance in Saccharomyces cerevisiae. Appl. Microbiol. Biotechnol., 97: 297-303.
Matsufuji Y, Nakagawa T, Fujimura S, Tani A, and Nakagawa J. 2010. Transcription factor Stb5p is essential for acetaldehyde tolerance in Saccharomyces cerevisiae. J. Basic Microbiol. 50: 494-498.
Matsufuji Y, Fujimura S, Ito T, Nishizawa M, Miyaji T, Nakagawa J, Ohyama T, Tomizuka N and Nakagawa T. 2008. Acetaldehyde tolerance in Saccharomyces cerevisiae involves the pentose phosphate pathway and oleic acid biosynthesis. Yeast. 25: 825-833.
発酵食品における発酵微生物の制御と機能の活用
日本各地、さらには世界各地には様々な発酵食品が受け継がれている。これら発酵食品は、微生物の存在を知る由もない私たち人類の先人達が試行錯誤の上、構築してきた技術であり、現在の科学でも未だ解明されていない優れた微生物機能と発酵菌叢の制御メカニズムにより成立している。
私たちは、日本酒醸造、ビール醸造、ワイン醸造、なれずしなど、人類が長い年月をかけて示してきた「発酵技術の粋」を科学的に解明したいと考えている。
特に以下の分野に関して研究を進めている。
1. 清酒酵母をはじめとした人類がドメスティケーション化してきた産業用酵母の進化の道筋の解明
2. 自然界に生息する野生酵母の新たな機能の発掘
3. ワインやなれずしなど自然発酵における微生物菌叢の変遷制御メカニズムと微生物機能の解明
4. 地域の伝統的発酵食品の文化的理解
参考文献
中川智行, 堀光代. 2025. 伝統的郷土料理「ナレズシ」の発酵科学, マイコトキシン, 75:2-2.(総説)
堀光代, 岩橋均, 中川智行. 2024. 岐阜市長良川の伝統的発酵食品「鮎鮨(鮎なれずし)」の発酵制御. 化学と生物. 62: 462-464.(総説)
Nakagawa T, Yoshimura A, Sawai Y, Hisamatsu K, Akao T, and Masaki K. 2024. Japanese sake making using wild yeasts isolated from natural environments. Biosci Biotechnol Biochem, 88: 231-236.(総説)
Hori M, Kawai Y, Noguchi K, Nakamura K, Shimada M, Iwahashi H, Nagakawa T. 2024. Antimicrobial activity and productivity of γ-aminobutyric acid in lactic acid bacteria isolated from traditional Gifu ayu-narezushi. Food Sci Technol Res, 30: 247-252.
Hori M, Kawai Y, Nakamura K, Shimada M, Iwahashi H, Nakagawa T. 2022. Characterization of the bacterial community structure in traditional Gifu ayu-narezushi (fermented sweetfish). J Biosci Bioeng, 134:331-337.
Doi R, Wu Y, Kawai Y, Wang L, Zendo T, Nakamura K, Suzuki T, Shimada M, Hayakawa T, and Nakagawa T. 2021. Transition and regulation mechanism of bacterial biota in Kishu saba-narezushi (mackerel narezushi) during its fermentation step. J Biosci Bioeng, 132: 606-612..
メチロトローフ酵母のメタノール代謝制御機構の解明
メタノールを唯一の炭素源・エネルギー源として利用できるメタノール資化性微生物は、メタノールが安価な炭素源であることなどから、異種遺伝子発現系の開発など応用利用に関する研究が盛んに行われている。また、近年、メタノール細菌が植物との共生関係を結んでいることが明らかとなり、植物の成長促進に関与するともいわれている。
当グループでは、メタノール資化性酵母のメタノール代謝制御機構、異種遺伝子発現系の開発、スーパーメタノール酵母の構築に向けた分子育種など、メタノール資化性酵母の分子育種と産業利用を目指している。
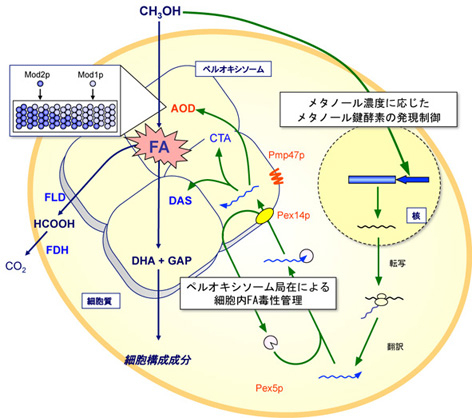
図. メチロトローフ酵母のメタノール代謝の制御メカニズム.
参考文献
中川智行. 2024. C1酵母の細胞内C1毒性管理と高メタノール環境に対する細胞適応の分子機構−環境循環型メタノールによる「バイオエコノミー」の実践に向けたC1酵母の細胞機能の開発. 化学と生物, 62: 233-239.(総説)
Cai HL, Shimada M, Nakagawa T. 2022. The potential and capability of the methylotrophic yeast Ogataea methanolica in a "methanol bio-economy. Yeast, 39:440-448.(総説)
Cai H-L, Shimada A, Hamaguchi T, Mizoguchi A, Yonekura K, Tsuchiyama K, Shimada M, Ebihara A, Tani K, Nakagawa T. 2026. In vitro and in vivo functional structures of alcohol oxidase isozymes in the methylotrophic yeast Ogataea methanolica. Microbial Biotechnol., 19: e70355.
Zhu J, Cai HL, Goto S, Shimada M, Yurimoto H, Sakai Y, Yoko-o T, Chiba Y, Nakagawa T. 2025. Physiological role of the FDH1 gene in methylotrophic yeast Komagataella phaffii and carbon recovery as formate during methylotrophic growth of the fdh1-deletion strain. J Biosci Bioeng, 139: 206-212.
Cai HL, Doi R, Shimada M, Hayakawa T, Nakagawa T. 2021. Metabolic regulation adapting to high methanol environment in the methylotrophic yeast Ogataea methanolica. Microbial Biotechnol, 14: 1512-1524.
メチロバクテリウム属細菌の植物共生メカニズムとレアアースによるメタノール代謝制御
近年、メタノールを唯一の炭素源として生育できるメチロバクテリウム属細菌が植物との共生関係を結んでいることが明らかとなり、その細胞機能が植物の成長促進に関与するともいわれている。
当グループでは、メタノール資化性細菌のレアアース特異的メタノール脱水素酵素の機能解明と植物との共生メカニズムの解明を目指している。また、根粒菌がレアアースを利用するメタノール代謝系を持つことを見いだし、その機能と役割を解析している。
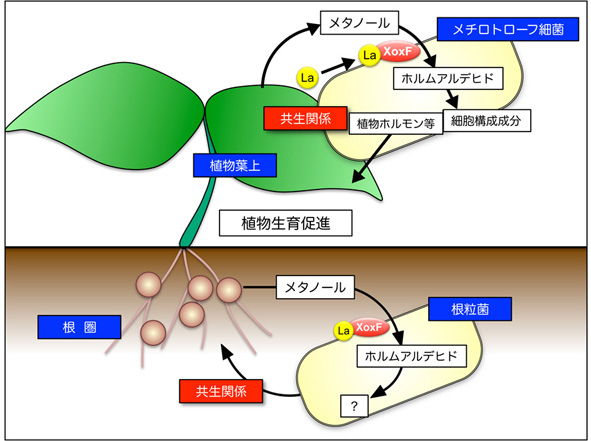
図. メチロバクテリウム細菌と根粒菌の植物共生とメタノール代謝の制御メカニズム.
参考文献
Pastawan V, Fitriyanto NA, Nakagawa T. 2020. Biological function of lanthanide in plant-symbiotic bacteria: Lanthanide-dependent methanol oxidation system. Rev Agric Sci, 8: 186-198.(総説)
Pastawan V, Suganuma S, Mizuno K, Wang L, Tani A, Mistui R, Nakamura K, Shimada M, Hayakawa T, Fitriyanto NA, Nakagawa T. 2020. Regulation of lanthanide-dependent methanol oxidation pathway in the legume symbiotic nitrogen-fixing bacterium Bradyrhizobium sp. strain Ce-3. J Biosci Bioeng, 130: 582-587.
Wang L, Hibino A, Suganuma S, Ebihara A, Iwamoto S, Mitsui R, Tani A, Shimada M, Hayakawa T, Nakagawa T. 2020. Preference for particular lanthanide species and thermal stability of XoxFs in Methyorubrum extorquens strain AM1. Enzyme Microb Technol, 136: 109518.
Wang L, Suganuma S, Hibino A, Mitsui R, Tani A, Matsumoto T, Ebihara A, Fitriyanto NA, Pertwiningrum A, Shimada M, Hayakawa T, Nakagawa T. 2019. Lanthanide-dependent methanol dehydrogenase from the legume symbiotic nitrogen-fixing bacterium Bradyrhizobium diazoefficiens strain USDA110. Enzyme Microb Technol, 130: 109371.
Nakagawa T, Mitsui R, Tani A, Sasa K, Tashiro S, Iwama T, Hayakawa T, Kawai K. 2012. A Catalytic Role of XoxF1 as La3+-Dependent Methanol Dehydrogenase in Methylobacterium extorquens Strain AM1. PLoS ONE 7: e50480.
産業用微生物の探索と育種
新たな機能をもつ微生物を自然界に広く求め、その微生物の持つ機能を酵素、遺伝子レベルで解析し、有用酵素を食品産業をはじめとした様々な産業に応用することを目指している。
参考文献
Nakagawa T, Ikehata R, Myoda T, Miyaji T and Tomizuka N. 2007. Overexpression and functional analysis of cold-active beta-galactosidase from Arthrobacter psychrolactophilus strain F2. Protein Expr. Purif. 54: 295-299.
Nakagawa, T., Fujimoto, Y., Ikehata, R., Miyaji, T. and Tomizuka, N. 2006. Purification and molecular characterization of cold-active beta-galactosidase from Arthrobacter psychrolactophilus strain F2. Appl. Microbiol. Biotechnol. 72: 720-725.
Nakagawa, T., Nagaoka, T., Miyaji, T. and Tomizuka, N. 2005. Cold-active polygalacturonase from psychrophilic-basidiomycetous yeast Cystofilobasidium capitatum strain PPY-1. Biosci. Biotechnol. Biochem. 69: 419-421